今回のパブリック・コメントは第1段階
昨年の23年12月に交付された新しい大麻法/麻向法では、2段階の改正がこれから施行されます。
厚労省方針
第一段階 24年10月1日
大麻由来医薬品の施用、施用罪の適用、CBD製品のTHC残留限度値の設定
大麻草研究栽培者免許の施行、分析業務は麻薬研究者(都道府県知事免許)
第二段階 25年3月1日
第一種、第二種、研究者の栽培規制に関すること
今回のパブリック・コメントは、第一段階となっています。締切6月29日まで
【募集開始】医療従事者/CBD製品事業者などの現場の声を届ける機会です。
https://hemptoday-japan.net/16244
THC分析法のガイドライン
これまでは、大麻製品の輸入を規制する2つの法律で次のように対応していました。
大麻取締法:成熟した茎と種子以外の大麻製品はNG
→ 茎および種子から製造されていることの製造証明書
麻薬及び向精神薬取締法:THCが含有されている製品はNG
→ THCが含有していないことの分析証明書(COA)
窓口は、関東信越厚生局麻薬取締部(https://www.ncd.mhlw.go.jp/cbd.html)で20年5月頃からCBD製品の輸入手続きが明確化されていました。しかし、「捜査上の明らかにできない」という理由から、CBD製品のTHC残留限度値は非公開なままでした。
輸入CBD製品ビジネスをしている方々の相場観は、分析証明書(COA)においてTHC濃度0.02%以下のLOD:Limit of Detection(検出限界)で運用されていると言われています。
海外の試験規格例
厚労省方針:Xevo TQ Absoluteの導入を推奨(最高機種!!)
こうした検査基準や手法などは、日本が独自に作成しなくても、下記のような国際標準規格を定めている団体で公表されている試験規格を採用/導入することができます。
ところが今回発表された厚生労働省の基準では、THC残留限度値を、こうした国際標準の1000倍以上厳しい1~10ppmに設定したため、Xevo TQ Absoluteの導入を推奨(最高機種)し、その分析手順が提示されています。
1)ASTMインターナショナル(国際標準化団体)
2017年にD37Cannbis技術委員会を設立して、栽培、品質保証、
試験所、包装、セキュリティ等の全分野の指針を開発
https://www.astmcannabis.org/committee-d37-on-cannabis/
2)AOACインターナショナル(化学分析標準化団体)
2019年~ 大麻分析科学プログラム(CASP):
試験所や製造業者が実施することが推奨される自主的な標準性能要件
(SMPR: Standard Method of Performance Requirements)を公表
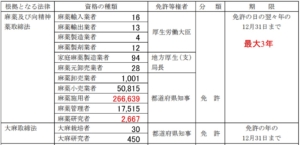
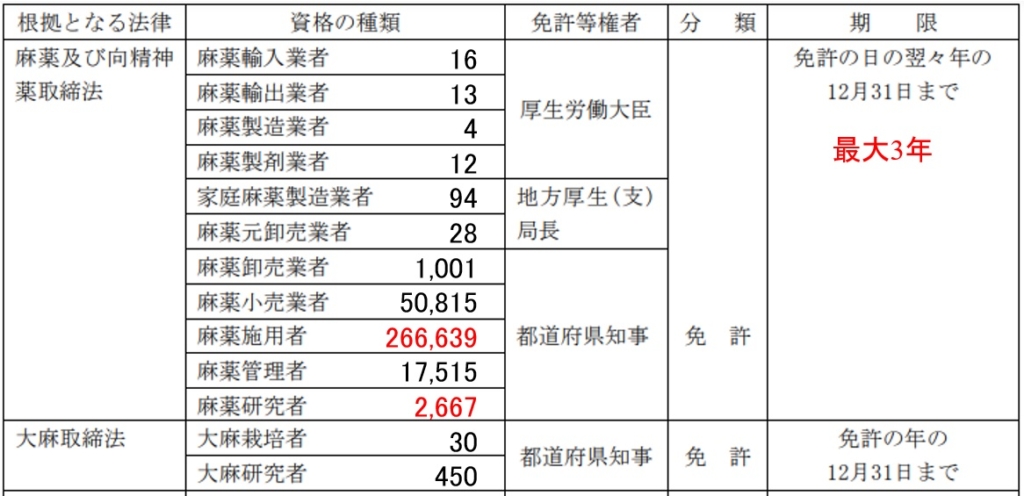
THCの検査は、麻薬研究者が担う。
これまでは検査業務に必須だった大麻研究者の免許は必要ではなく、栽培を伴う研究に「大麻草栽培研究者」免許が創設されました。24年10月1日以降は、「麻薬研究者」が大麻草やカンナビノイド製品(CBD製品)の検査業務を取り扱えるようになります。全国で約2600名います。
但し、今回のパブコメの方針には、国内の登録検査機関の要件は発表されていません。これは第2段目のパブコメの項目となっています。

図1 全国の麻薬取扱者および大麻取扱者の人数 引用:麻薬・覚醒剤行政の概況(2022)
最も大きな課題、標準品の入手が無視されている
今まで国際条約における禁止品としての対象であったため、分析試験に必要な認証標準物質(CRM, Certificated Reference Material)の入手が極めて困難な状態が続いています。
標準品とは、わかりやすくいうと、CBD製品にTHCがどれぐらい残留しているかを分析するときに使う「ものさし」のようなものです。物の長さを測る時には、「ものさし」がないと、対象物が何㎜なのか正確に測れません。化学分析装置において標準品の入手は必須事項なのです。
米国の試薬製造販売会社Cerilliant(セリリアント)のHPには、Δ9-THC試薬 T-005-1ML
メタノール中 1.0 mg/mL :35ドル(約5250円)で購入可能と書いてあります。
しかし、これが日本に輸入するとなると、約100万円(2023年冬)でしか入手できません。
この件については、「ネットで買える「大麻成分グミ」を食べてみた! その正体は?規制対象ではない理由に分析から迫る! 井之上 浩一(立命館大学薬学部教授)による「現代ビジネス」の記事によって、次のように指摘されています。
分析するためには、標準品が必要です。CBDはよいのですが、粗悪品を検査するには必ずTHCも分析する必要があります。
このTHCは麻薬の主犯なので、研究者とはいえ簡単に入手できません。麻薬取扱者免許の取得、金庫の設置、諸手続きなどをすべて済ませて、やっと注文ができる状況です。
これが麻薬取扱者の免許です(表面のみ、一部加工済み)
また、仮に注文しても、国内企業では取り扱っていないので、海外からの輸入になります。
これには半年以上かかります。
さらに、問題は金額です! 内緒ですが、THC標準品はそんなに高くはありません(1万円程度)、ただし、運搬や輸入手続きで50倍に跳ね上がります。
そんな手間暇をかけて、分析の準備をしますが、この後も難しい。(以下、省略)
パブコメ意見例
それでは、この分析に関するパブリックコメントには、どのような内容で投稿したらよいでしょうか?
以下に例文を挙げますので、参考にしてみてください。
今回のΔ9-THCの分析法では、分析業務に必須となるΔ9-THC標準品の入手については特に書いていませんでした。井之上浩一(立命館大学薬学部教授)による「現代ビジネス」の記事(https://gendai.media/articles/-/73849)によると、標準品の入手が困難で、価格が50倍以上という指摘がされています。また、最近の相場では試薬会社から1本(1mL )100万円で購入予算を確保してほしいという話を聞きます。日本における検査業務の体制を整備するにあたって、国内試薬会社等の協力により、国産のTHC標準品を確保できるように、国が検査体制の整備の一環として積極的に関与すべきです。
●年●月●日
氏名、住所、メール
今回の対象パブコメ
「大麻由来製品に含まれるΔ9-THC の標準的な分析法(案)」に関する御意見の募集について
案件番号495240037
案の公示日2024年5月30日
受付締切日時2024年6月29日0時0分
所管省庁厚生労働省
こちらから(外部サイトへのリンク):https://public-comment.e-gov.go.jp/495240037
参考リンク
大麻草の栽培の規制に関する法律、麻薬及び向精神薬取締法を一部改正する法律
第一段 未施行 医薬品の解禁と施用罪の適用
https://elaws.e-gov.go.jp/document?lawid=323AC0000000124_20250601_504AC0000000068
第二段 未施行 産業用と医療用の栽培の適正化
https://elaws.e-gov.go.jp/document?lawid=323AC0000000124_20251212_505AC0000000084