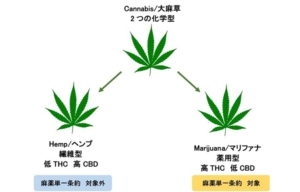
メディケアのヘンプを容認
米国の連邦判事は、反嗜好用大麻団体が提訴している訴訟の結論が出るまでの間、一定のヘンプ由来製品をメディケアの実証プログラムで使用することを認める判断を下した。
この判断により、米国医療保険制度を管轄するCenters for Medicare & Medicaid Services(CMS)が進める本プログラムは、法的争いが続く中でも開始が可能となる。
判決では、原告側が求めていたプログラム開始前の差し止め(緊急停止要請)は却下された。ただし訴訟自体は継続しており、最終的な判断には数カ月を要する可能性がある。
今回の動きに対しては、反嗜好用大麻団体に加え、医薬品開発企業からも反発が出ている。特に、非酩酊性のヘンプ製品を限定的に医療現場で利用可能とするこの仕組みは、CBD関連事業者にとっては大きな恩恵となる可能性があるため、注目が集まっている。
「規制の抜け道」との批判
「これはイノベーションではなく、規制の抜け道に過ぎない」と、ワシントンD.C.を拠点とするMMJ International HoldingsのCEO、Duane Boise氏は述べた。同社はカンナビノイド医薬品の開発を進めている。
Boise氏は、政府が2つの異なる制度を同時に運用していると批判する。ひとつは長年の臨床試験と厳格な規制審査を必要とする医薬品ルート、もうひとつはCMSの枠組みを通じて消費者向けヘンプ製品を医療現場に導入するルートである。
訴訟を起こした反嗜好用大麻団体は、この政策が米国食品医薬品局(FDA)の医薬品承認制度を形骸化させると主張している。また一部の批評家は、公衆衛生リスクや連邦政府の権限逸脱の問題としても捉えている。
主な原告であるSmart Approaches to Marijuanaは、このCMSの取り組みを「反科学的であり、連邦法違反の可能性が高い」と批判し、「公衆衛生に深刻な影響を及ぼす」と警告している。
適用範囲の限定性
一方、連邦当局は、こうした批判は制度の内容を誤解していると反論している。本プログラムはごく限られた実証プロジェクトにのみ適用されるものであり、ヘンプ製品をメディケアが直接給付対象とするものではないとしている。
また政府は裁判資料の中で、反対派がヘンプと嗜好用大麻を混同している点を指摘し、2018年の農業法(Farm Bill)によりヘンプは規制薬物から除外されているという法的区別を無視していると主張している。
さらに、原告側が主張する経済的損害についても、まだ参入していない市場での損害を根拠にしている点に疑問を呈している。
編集部あとがき
今回の記事を以下、4つのポイントに整理しましたのでご参考ください。
1.ヘンプ医療導入は「限定的にスタート」した
裁判所はプログラムの即時停止を認めず、ヘンプ製品を用いたメディケア実証は開始可能となった。ただし本格的な制度化ではなく、あくまでテスト段階にとどまる。
2.CBD業界にとっては大きな追い風
非酩酊性ヘンプ製品の医療現場への導入は、特にCBD事業者にとって新たな市場機会となる可能性があり、業界の関心が高まっている。
3.医薬品業界との「構造的対立」が顕在化
医薬品開発企業は、臨床試験を経るルートと消費者製品ルートの二重構造を問題視している。規制の公平性を巡る対立が今後さらに激化する可能性がある。
4.法的・規制的な決着はまだ先
今回の判断はあくまで暫定的なものであり、訴訟は継続中。最終的な規制の方向性は今後数カ月の司法判断に委ねられている。